Lumasiran heisst das Wundermittel, das zur Behandlung von Primärer Hyperoxalurie Typ 1 verfügbar ist. Die Wirksam- und Verträglichkeit wurde in einer internationalen Studie mit Beteiligung des Inselspitals, des Universitätsspitals Bern und der Universität Bern nachgewiesen. Damit steht erstmals eine Kausaltherapie für die sehr seltene Stoffwechselkrankheit zur Verfügung, teilt die Inselgruppe mit.
Das verursacht Primäre Hyperoxalurie Typ 1
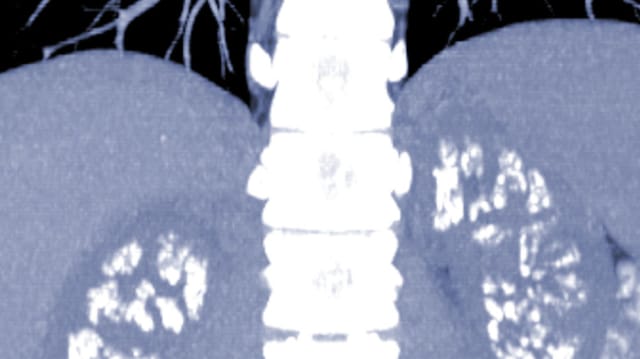
Die sehr seltene Krankheit «Primäre Hyperoxalurie Typ 1» (PH1) ist eine genetisch bedingte Stoffwechselkrankheit, die auf den Ausfall eines Enzyms zum Abbau von Fettsäuren zurückgeht. Durch eine hohe Konzentration von Oxalsäure in Verbindung mit Calcium kommt es in der Niere – und anderen Organen – zur Bildung von Calciumoxalsäure-Kristallen (Nierensteinen).
Diese können die Nierenfunktion vermindern und zu einer Niereninsuffizienz bis hin zum Ausfall der Nierenfunktion führen. PH1 tritt in vielen unterschiedlichen Formen in unterschiedlichen Altersgruppen auf und gilt als deutlich «unterdiagnostiziert». Studien schätzen die Häufigkeit von PH1 auf etwa eine betroffene Person pro 150 000 Einwohner. Bisher bestand die einzige Kausaltherapie in einer Lebertransplantation.
Medikament sorgt für normale Werte
In der jüngst im Fachjournal New England Journal of Medicine publizierten
Studie berichten die Forschenden von einer neuen Therapie, die PH1 medikamentös erfolgreich behandeln kann. «Die sehr gute Verträglichkeit und das Ausmass der Oxalsäurereduktion waren sehr positiv. Es traten keine schwerwiegenden Nebenwirkungen auf, die meisten Patientinnen und Patienten hatten nach sechs Monaten mit Lumasiran normale normale Oxalsäurewerte in Blut und Urin», erläutert Professor Daniel Fuster vom Inselspital, Universitätsspital Bern.
Professor Daniel Fuster, Leitender Arzt Universitätsklinik für Nephrologie am Inselspital, Universitätsspital Bern und Gruppenleiter am Department for BioMedical Research (DBMR) der Universität Bern. (zvg)
Studie erfolgte in 16 Zentren
Die Publikation entstammt der «
Illuminate-A-Studie», einer internationalen, randomisierten, Placebo kontrollierten Doppelblindstudie. Sie wurde an 16 Zentren unter anderem in den USA, Frankreich, Deutschland, Grossbritannien und der Schweiz ausgeführt.
Sie schloss 39 Patientinnen und Patienten (Alter über 6 Jahre) ein. 13 Personen erhielten Placebo, 26 wurden mit Lumasiran behandelt. Die Inselgruppe bezeichnet die oben erwähnten Resultate als bahnbrechend.
Seit November 2020 ist Lumasiran zur Behandlung von PH1 in den USA und der EU zugelassen. In der Schweiz steht die Zulassung noch aus. Am Inselspital sind derzeit sechs Patientinnen und Patienten, darunter zwei Kinder, in Behandlung.
Die nächste Schritte
Wie der Mitteilung der Inselgruppe zu entnehmen ist, braucht die Diagnose und Therapie viel Erfahrung sowie ein spezialisiertes, interdisziplinäres Team. International würden erst wenige Zentren zur Verfügung stehen, die den hohen Anforderungen gerecht werden.
Um alle Partner auf die speziellen Anforderungen vorzubereiten, werden Aus- und Weiterbildungen notwendig sein. Aufgrund der Teilnahme an der Illuminate-A-Studie und den damit verbundenen Erfahrungen mit der Lumasirantherapie seien die Fachleute am Inselspital, Universitätsspital Bern dazu gerüstet.