Darüber hinaus zeichnen sich klinische Studien durch ihre Komplexität aus - von der sorgfältigen Standortauswahl und der anspruchsvollen Rekrutierung von Probanden bis hin zur präzisen Studienüberwachung, effektivem Datenmanagement und strikter Einhaltung von Vorschriften.
Die Senkung der Entwicklungskosten für Kosten für neue Geräte und Therapien hängt maßgeblich von effizienter Datennutzung und -verarbeitung ab. Allerdings werden diese Fortschritte häufig durch veraltete klinische Systeme, begrenzte Ressourcen und isolierte Prozesse behindert, was sich nachteilig auf die Durchführung von Studien, die Transparenz, den Datenaustausch und die Zusammenarbeit auswirken kann.
Eine kürzlich durchgeführte Studie unter führenden Fachleuten aus der Medizintechnik gibt Aufschluss über den aktuellen
Stand der klinischen Forschung.
Ergebnisse der klinischen Benchmark-Studie
Die Studienergebnisse zeigen, dass die digitale Verwaltung interner Systeme für 45% der Befragten eine strategische Priorität darstellt.
Darüber hinaus haben mehr als 50% der Befragten bereits mindestens eine digitale Anwendung im Einsatz. Trotz positiver Fortschritte bei der Technologieeinführung sind manuelle Arbeitsabläufe, isolierte Prozesse und Datenbeschränkungen in vielen der befragten Unternehmen immer noch an der Tagesordnung.
Kevin Liang, VP of Vault Clinical Strategy bei Veeva MedTech, betont, dass die Medizintechnikbranche jetzt die Chance hat, klinische Systeme zu modernisieren, um einen schnelleren Zugang zu Studiendaten zu ermöglichen. Die Einführung digitaler klinischer Systeme kann die Zusammenarbeit, die Studieneffizienz, die Produktivität und die Einhaltung von Vorschriften verbessern, was letztendlich zu mehr Innovation und einer qualitativ besseren Patientenversorgung führt.
Überwindung von Ressourcenbeschränkungen
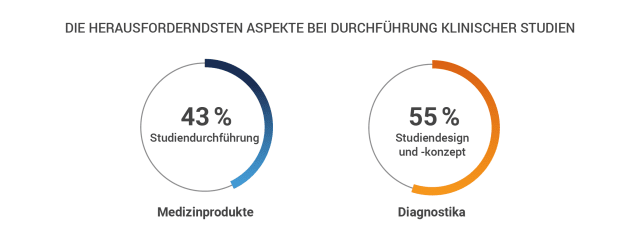
55 % der Befragten gaben an, dass die Durchführung klinischer Studien für Medizintechnikunternehmen aufgrund von Herausforderungen in den Bereichen Personal, Material und Arbeitseffizienz eine bedeutende Schwierigkeit darstellt. Zudem empfinden Experten aus der Medizintechnik die Standortwahl, den Aufbau, Vertragsverhandlungen und die Personalschulung als einige der anspruchsvollsten Aspekte bei klinischen Studien (43%). Fachleute im Bereich Diagnostik hingegen betrachten das Studiendesign und -konzept als die größten Hürden (55%).
Die Haupterkenntnis, die aus den Ergebnissen hervorgeht, unterstreicht die deutliche Notwendigkeit für die Medizintechnik, ihre Prozesse zu überdenken und unnötige Aktivitäten im Kontext klinischer Betriebsabläufe und Studiendurchführung zu eliminieren.
Durch die Implementierung von technologischen Lösungen, die Prozesse, Dokumentation und Studienmanagement automatisieren und optimieren, haben Unternehmen die Möglichkeit, ihre Effizienz signifikant zu erhöhen, ohne zusätzliche Ressourcen dafür aufwenden zu müssen.
Proaktive regulatorische Anpassungen vor und nach der Markteinführung: Ein evidenzbasierter Ansatz
Die zunehmenden regulatorische Anforderungen, die eine verstärkte Datenbereitstellung fordern, zwingen Unternehmen der Medizintechnik- und Diagnostikbranche dazu, ihre klinischen Aktivitäten zu intensivieren. Im Kontext der EU-MDR und IVDR der EU sind Hersteller von Medizinprodukten zudem verpflichtet, zusätzlcihe Nachweise vor und nach der Markteinführung bzw. dem Inverkehrbringen vorzulegen.
Gegenwärtig setzen 21% der Befragten Real-World Evidence (RWE), gefolgt von Literaturrecherchen und vergleichenden Studien (20%), um zusätzliche Informationen über bereits existierende Produkte auf dem EU-Markt zu sammeln und die PMCF/PMPF-Anforderungen zu erfüllen. Dies verlangsamt jedoch den Studienablauf und die Datenanalyse, was zu einer erhöhten zeitlichen und finanziellen Belastung für den Abschluss der Studienaktivitäten führt.
Um sowohl eine fortlaufende Datenstandardisierung als auch den reibungslosen Marktzugang für Produkte sicherzustellen, ist es unabdingbar, eine solide PMCF/PMPF-Strategie frühzeitig in den klinischen Studienplan zu integrieren. Dazu zählen die klare Definition eines durchgängigen Prozesses, eine kollaborative Zusammenarbeit über Funktionsbereiche hinweg und eine interaktive Vernetzung über verschiedene Standorte hinweg.
In einer Zeit, in der Daten aus dem Alltagsgeschehen immer stärker gefragt sind, gewinnt die Integration digitaler Technologien in klinische Abläufe und die Verwaltung von Studiendaten zur Schaffung einer einheitlichen Datenquelle zunehmend an Bedeutung. Diese Entwicklung ist entscheidend für die erfolgreiche Erteilung behördlicher Zulassungen.
Unternehmen wie
Cook Research,
Terumo Europe und viele andere setzen auf Cloud-Plattformen wie
Veeva Vault CTMS und
eTMF, um Datenanforderungen zu erfüllen, klinische Studien zu beschleunigen und die Einhaltung von Vorschriften in mehreren Ländern zu gewährleisten. Gleichzeitig bieten diese Plattformen die erforderliche Flexibilität, um die Unternehmen vor zukünftigen regulatorischen Änderungen zu schützen.
Effizienzsteigerung durch den Einsatz von Technologie
Die digitale Transformation spielt eine wesentliche Rolle bei der Optimierung der klinischen Forschung in der Medizintechnik. Die Umfrage verdeutlicht, dass Unternehmen zwar in Richtung digitaler Prozesse voranschreiten, jedoch nach wie vor einige Herausforderungen bei der Systemanwendung bestehen.
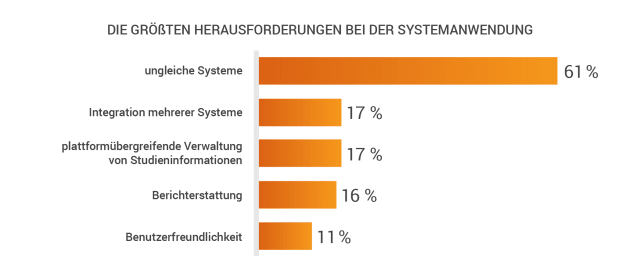
Über 61% der Befragten berichteten von Schwierigkeiten im Umgang mit unterschiedlichen Systemen. Hierbei wurden insbesondere die Integration mehrerer Systeme (17%), die plattformübergreifende Verwaltung von Studieninformationen (17%), die Berichterstattung (16%) und die Benutzerfreundlichkeit (11%) als die größten Herausforderungen im Bereich klinischer Anwendungen aufgeführt.
Um diese Herausforderungen zu bewältigen, ist es für die Medizintechnikvon entscheidender Bedeutung, einen ganzheitlichen Ansatz für ihre klinischen Prozesse und die zugehörigen Ökosysteme zu verfolgen. Mit der Expertise eines klinischen Technologiepartners können Unternehmen sicherstellen, dass das System ihre unternehmensspezifischen Anforderungen unterstützt, die Zusammenarbeit erleichtert und den Echtzeit-Datenaustausch zwischen allen Beteiligten ermöglicht.
Auf dem Weg in eine papierlose Zukunft
Die Mehrheit der befragten Unternehmen ergreift Maßnahmen, um digitale, patientenzentrierte Studien zu ermöglichen. 45% der Befragten planen, in den kommenden 12 Monaten die digitale Verwaltung interner Systeme als höchste Priorität zu setzen, während zusätzliche 14% Pläne zur Einführung von Fernüberwachungslösungen angaben.
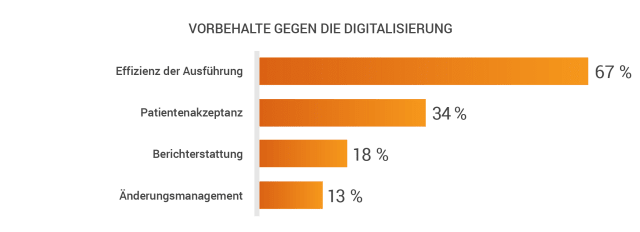
Trotz der positiven Entwicklungen gibt es noch einige Herausforderungen zu bewältigen. 67% der Teilnehmer gaben an, dass die Effizienz der Umsetzung das größte Problem bei der Einführung digitaler Technologien darstellt. Zudem wurden die Patientenakzeptanz (34%), die Datenerfassung und -berichterstattung (18%) sowie das Änderungsmanagement (13%) als die zentralen zu erwartenden Herausforderungen genannt.
Die Einführung digitaler und hybrider Studien erfordert Zeit. Die Festlegung einer klaren Strategie und einer Roadmap für die digitale Transformation basierend auf Geschäftsanforderungen, Prozessen und Zielen kann Unternehmen dabei unterstützen, die damit einhergehenden Herausforderungen zu bewältigen, neue Technologien einzuführen und eine schnellere Systemreife zu erreichen.
Fazit
In letzten Jahren haben sich klinische Studien im Bereich der Medizintechnik deutlich komplexer entwickelt und erfordern eine bisher beispiellose Menge an Datenerfassung und -analyse. Um mit diesen Anforderungen Schritt zu halten, müssen Unternehmen ihre Prozesse kontinuierlich optimieren, Ressourcen effizient einsetzen und in moderne cloudbasierte Anwendungen investieren.
Durch die Identifizierung von Lösungen zur Bewältigung von Ressourcenknappheit, standortübergreifender Zusammenarbeit, regulatorischen Änderungen und zur Integration neuer Technologien kann die Medizintechnik die Produktentwicklung beschleunigen, die Datenintegrität sicherstellen und die notwendige Flexibilität erlangen, um unvorhergesehene Entwicklungen erfolgreich zu bewältigen.
Die Zukunft der klinischen Forschung liegt in der digitalen Transformation und in patientenzentrierten Ansätzen, um die Effizienz zu steigern, die Ergebnisse für die Patienten zu verbessern und sichere und wirksame Medizinprodukte und Diagnostika für den Markt bereitzustellen.
Laden Sie den vollständigen Bericht herunter, um detaillierte Einblicke in die aktuellen Trends und Herausforderungen im Management klinischer Studien zu erhalten sowie zu erfahren, wie die
Veeva MedTech Clinical Suite Sie dabei unterstützen kann, klinische Daten und Prozesse zu vereinheitlichen, um Produkte schneller und effizienter für die Patienten zugänglich zu machen.